NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Thank you for reading this post, don't forget to subscribe!Important Questions of Class 10 Chapter 2 Acids Bases and Salts अम्ल, क्षारक एवं लवण

Page No. 18
Question 1:
You have been provided with three test tubes. One of them contains distilled water and the other two contain an acidic solution and a basic solution, respectively. If you are given only red litmus paper, how will you identify the contents of each test tube?
आपको तीन परखनालियाँ दी गई हैं| इनमे से एक में आसवित जल एवं शेष दो में से एक में अम्लीय विलयन तथा दुसरे में क्षारीय विलयन है| यदि आपको केवल लाल लिटमस पात्र दिया जाता है तो आप प्रत्येक परखनली में रखे गए पदार्थों की पहचान कैसे करेंगे?
Answer
(1) If the colour of red litmus does not change then it is acid.
(2) If the colour of red litmus changes to blue then it is base.
(3) If there is slight change in the colour of red litmus (such as purple) then it is distilled water.
(1) यदि लाल लिटमस पत्र का रंग नहीं बदलता तो यह अम्ल है|
(2) यदि लाल लिटमस पत्र का रंग नील रंग में परिवर्तित हो जाता है तो यह क्षारक है|
(3) यदि लिटमस पत्र के रंग में हल्का परिवर्तन (हलके बैंगनी) होता है तो यह आसवित जल है|
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Page No. 22
Question 1:
Why should curd and sour substances not be kept in brass and copper vessels?
पीतल एवं तांबे के बर्तनों में दही एवं खट्टे पदार्थ क्यों नहीं रखने चाहिए?
Answer
Curd and other sour substances contain acids. Therefore, when they are kept in brass and copper vessels, the metal reacts with the acid to liberate hydrogen gas and harmful products, thereby spoiling the food.
दही एवं खट्टे पदार्थों में अम्ल पाया जाता है| इस प्रकार जब इन पदार्थों को पीतल एवं तांबे के बर्तनों में रखा जाता है तो धातु अम्ल के साथ अभिक्रिया कर हाइड्रोजन गैस और हानिकारक उत्पाद मुक्त करते हैं जिससे भोजन ख़राब हो जाता है|
Question 2:
Which gas is usually liberated when an acid reacts with a metal? Illustrate with an example. How will you test for the presence of this gas?
धातु के साथ अम्ल की अभिक्रिया होने पर सामान्यतः कौन सी गैस निकलती है? एक उदहारण के द्वारा समझाइए| इस गैस की उपस्थिति की जाँच आप कैसे करेंगे?
Answer
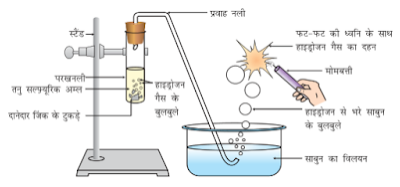
Hydrogen gas is usually liberated when an acid reacts with metal.
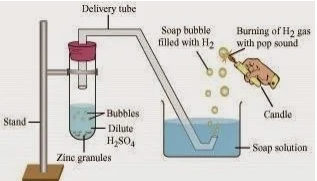
धातु के साथ अम्ल की अभिक्रिया होने पर सामान्यतः हाइड्रोजन गैस निकलती है|
Question 3:
Metal compound A reacts with dilute hydrochloric acid to produce effervescence. The gas evolved extinguishes a burning candle. Write a balanced chemical equation for the reaction if one of the compounds formed is calcium chloride.
कोई धातु यौगिक ‘A’ तनु हाइड्रोक्लोरिक अम्ल के साथ अभिक्रिया करता है तो बुदबुदाहट उत्पन्न होती है| इससे उत्पन्न गैस जलती मोमबत्ती को बुझा देती है| यदि उत्पन्न यौगिकों में एक से कैल्सियम क्लोराइड हैं, तो इस अभिक्रिया के लिए संतुलित रासायनिक समीकरण लिखिए|
Answer
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + CO2 (g) + H2O (l)
Calcium Carbonate + Hydrochloric acid → Calcium Chloride + Carbon dioxide + Water
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + CO2 (g) + H2O (l)
कैल्सियम कार्बोनेट + हाइड्रोक्लोरिक अम्ल → कैल्सियम क्लोराइड + कार्बन डाइऑक्साइड + जल
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Page No. 24
Question 1:
Why do HCl, HNO3, etc., show acidic characters in aqueous solutions while solutions of compounds like alcohol and glucose do not show acidic character?
HCl, HNO3 आदि जलीय विलयन में अम्लीय अभिलक्षण क्यों प्रदर्शित करते हैं, जबकि एल्कोहोल एवं ग्लूकोज जैसे यौगिकों के विलयनों में अम्लीयता के अभिलक्षण नहीं प्रदर्शित होते हैं?
Answer
When HCl or HNO3 are mixed with water then they dissolve in water to form H+ or H3O+ ions which shows their acidic character.
For example just see the following reactions
HCl (aq) → H+ + Cl–
H+ + H2O → H3O+When alcohols and glucose are mixed with water then they do not dissolve to form ions. Hence they do not show acidic character.
जब HCl या HNO3 को जल में घोला जाता है तो यह जल में घुलकर हाइड्रोजन आयन उत्पन्न करते हैं, जो उनके अम्लीय गुण को प्रदर्शित करता है| उदाहरण के लिए निम्नलिखित अभिक्रिया को देखें:
HCl (aq) → H+ + Cl–
H+ + H2O → H3O+
जबकि एल्कोहोल एवं ग्लूकोज जैसे यौगिक जल में घुलने पर हाइड्रोजन आयन उत्पन्न नहीं करते हैं, इस प्रकार यह अम्लीय गुण को प्रदर्शित नहीं करता|
Question 2:
How is the concentration of hydroxide ions (OH–) affected when excess base is dissolved in a solution of sodium hydroxide?
जब सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं तो हाइड्रॉक्साइड आयन (OH–) की सांद्रता कैसे प्रभावित होती है?
Answer
The concentration of hydroxide ions (OH−) would increase when excess base is dissolved in a solution of sodium hydroxide.
सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं तो हाइड्रॉक्साइड आयन (OH–) की सांद्रता बढ़ जाएगी|
Question 3:
Why does an aqueous solution of an acid conduct electricity?
अम्ल का जलीय विलयन क्यों विद्युत् का चालन करता है?
Answer
The presence of hydrogen (H+) or hydronium (H3O+) ions in the aqueous solution of an acid are responsible for conducting electricity.
अम्ल के जलीय विलयन में हाइड्रोजन ( H+) या हाइड्रोनियम आयन ( H3O+) की उपस्थिति के कारण विद्युत् का चालन होता है|
Question 4:
Why does dry HCl gas not change the colour of the dry litmus paper?
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को क्यों नहीं बदलती है?
Answer
Dry HCl gas not change the colour of the dry litmus paper because it has no Hydrogen ions (H+) in it.
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को नहीं बदलती है क्योंकि इसमें हाइड्रोजन आयन अनुपस्थित रहता है|
Question 5:
While diluting an acid, why is it recommended that the acid should be added to water and not water to the acid?
अम्ल को तनुकृत करते समय यह क्यों अनुशंसित करते हैं कि अम्ल को जल में मिलाना चाहिए, न कि जल को अम्ल में?
Answer
Since the process of dissolving an acid in water is exothermic, it is always recommended that acid should be added to water. If it is done the other way, then it is possible that because of the large amount of heat generated, the mixture splashes out and causes burns.
जल में अम्ल के घुलने की प्रक्रिया अत्यंत ऊष्माक्षेपी होती है| अम्ल को सदैव धीरे-धीरे तथा जल को लगातार जल में हिलाते हुए जल में मिलाना चाहिए| सांद्र अम्ल में जल मिलाने पर उत्पन्न हुई ऊष्मा के कारण मिश्रण आस्फलित होकर बाहर आ सकता है तथा आप जल सकते हैं
Question 6:
How is the concentration of hydronium ions (H3O+) affected when a solution of an acid is diluted?
अम्ल के विलयन को तनुकृत करते समय हाइड्रोनियम आयन ( H3O+) की सांद्रता कैसे प्रभावित हो जाती है?
Answer
When an acid is diluted, the concentration of hydronium ions (H3O+) per unit volume decreases. This means that the strength of the acid decreases.
जब अम्ल के विलयन को तनुकृत किया जाता है तब हाइड्रोनियम आयन ( H3O+) की सांद्रता में प्रति इकाई आयतन में कमी हो जाती है| इसका अर्थ है कि अम्ल की शक्ति घटती है|
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Page No. 28
Question 1:
You have two solutions, A and B. The pH of solution A is 6 and pH of solution B is 8. Which solution has more hydrogen ion concentration? Which of this is acidic and which one is basic?
आपके पास दो विलयन ‘A’ एवं ‘B’ हैं| विलयन ‘A’ के pH का मान 6 है एवं विलयन ‘B’ के pH का मान 8 है| किस विलयन में हाइड्रोजन आयन की सांद्रता अधिक है? इनमे से कौन अम्लीय है तथा कौन क्षारकीय है?
Answer
A pH value of less than 7 indicates an acidic solution, while greater than 7 indicates a basic solution. Therefore, the solution with pH = 6 is acidic and has more hydrogen ion concentration than the solution of pH = 8 which is basic.
7 के कम pH का मान अम्लीय विलयन को दर्शाता है तथा 7 से अधिक pH का मान क्षारकीय विलयन को दर्शाता है| | विलयन ‘A’ के pH का मान 6 है इसलिए यह अम्लीय है और इसमें विलयन ‘B’ की अपेक्षा हाइड्रोजन आयन की सांद्रता अधिक है| विलयन ‘B’ के pH का मान 8 है इसलिए यह क्षारकीय है|
Question 2:
What effect does the concentration of H+(aq) ions have on the nature of the solution?
H+ (aq) आयन की सांद्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है?
Answer
If the concentration of H+ (aq) ions is increased (>10-7) then the solution become acidic and if the concentration of H+ (aq) ions is decreased (<10-7) then the solution become basic in nature.
जब H+ (aq) आयन की सांद्रता (>10-7) बढ़ाई जाती है तो विलयन अम्लीय हो जाता है, और जब H+ (aq) आयन की सांद्रता (<10-7) घटाई जाती है तो विलयन की प्रकृति क्षारकीय हो जाता है|
Question 3:
Do basic solutions also have H+(aq) ions? If yes, then why are these basic?
क्या क्षारकीय विलयन में H+(aq) आयन होते हैं? अगर हाँ, तो यह क्षारकीय क्यों होते हैं?
Answer
Yes, basic solution also has H+ ions. However, their concentration is less as compared to the concentration of OH– ions that makes the solution basic.
हाँ, क्षारकीय विलयन में H+(aq) आयन होते हैं| OH- आयन के सांद्रता की तुलना में H+(aq) आयन की सांद्रता कम होती है जो विलयन को क्षारकीय बनाता है|
Question 4:
Under what soil condition do you think a farmer would treat the soil of his fields with quick lime (calcium oxide) or slaked lime (calcium hydroxide) or chalk (calcium carbonate)?
कोई किसान खेत की मृदा की किस परिस्थिति में बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड), बुझा हुआ चूना (कैल्सियम हाइड्रॉक्साइड) या चाक (कैल्सियम कार्बोनेट) का उपयोग करेगा?
Answer
If the soil is acidic and improper for cultivation, then to increase the basicity of soil, the farmer would treat the soil with quick lime or slaked lime or chalk.
यदि मृदा अम्लीय है और खेती के लिए अनुपयुक्त है तो किसान मृदा की क्षारकता बढ़ाने के लिए बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड), बुझा हुआ चूना (कैल्सियम हाइड्रॉक्साइड) या चाक (कैल्सियम कार्बोनेट) का उपयोग करेगा
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Page No. 33
Question 1:
What is the common name of the compound CaOCl2?
CaOCl2 यौगिक का प्रचलित नाम क्या है?
Answer
Bleaching Powder.
ब्लीचिंग पाउडर
Question 5:
Write an equation to show the reaction between Plaster of Paris and water.
प्लास्टर ऑफ़ पेरिस की जल के साथ अभिक्रिया के लिए समीकरण लिखिए|
Answer

Question 2:
Name the substance which on treatment with chlorine yields bleaching powder.
उस पदार्थ का नाम बताइए जो क्लोरीन से क्रिया करके विरंजक चूर्ण बनाता है|
Answer
Calcium hydroxide [Ca(OH)2]
कैल्सियम हाइड्रॉक्साइड [Ca(OH)2]
Question 3:
Name the sodium compound which is used for softening hard water.
कठोर जल को मृदु करने के लिए किस सोडियम यौगिक का उपयोग किया जाता है?
Answer
Washing soda (Na2CO3.10H2O)
वाशिंग सोडा (Na2CO3.10H2O)
Question 4:
What will happen if a solution of sodium hydrocarbonate is heated? Give the equation of the reaction involved.
सोडियम हाइड्रोकार्बोनेट के विलयन को गर्म करने पर क्या होगा? इस अभिक्रिया के लिए समीकरण लिखिए|
Answer
When sodium hydrogen carbonate is heated then sodium carbonate and water is formed along with the evolution of carbon dioxide gas.
सोडियम हाइड्रोकार्बोनेट के विलयन को गर्म करने पर सोडियम कार्बोनेट और जल के निर्माण के साथ कार्बन डाईऑक्साइड गैस उत्पन्न होता है|

NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Page No. 34
Question 1:
A solution turns red litmus blue, its pH is likely to be
कोई विलयन लाल लिटमस को नीला कर देता है, इसका pH संभवतः क्या होगा?
(a) 1 (b) 4 (c) 5 (d) 10
Answer
(d) 10
Question 2:
A solution reacts with crushed egg-shells to give a gas that turns lime-water milky. The solution contains
कोई विलयन अंडे के पिसे हुए कवच से अभिक्रिया कर एक गैस उत्पन्न करता है जो चूने के पानी को दुधिया कर देती है| इस विलयन में क्या होगा?
(a) NaCl (b) HCl (c) LiCl (d) KCl
Answer
(b) HCl
Question 3:
10 mL of a solution of NaOH is found to be completely neutralised by 8 mL of a given solution of HCl. If we take 20 mL of the same solution of NaOH, the amount HCl solution (the same solution as before) required to neutralise it will be
NaOH का 10 mL विलयन, HCl के 8 mL विलयन से पूर्णतः उदासीन हो जाता है| यदि हम NaOH के उसी विलयन का 20 mL लें तो इसे उदासीन करने के लिए HCl के उसी विलयन की कितनी मात्रा की आवश्यकता होगी?
(a) 4 mL (b) 8 mL (c) 12 mL (d) 16 mL
Answer
(d) 16 mL
Question 4:
Which one of the following types of medicines is used for treating indigestion?
(a) Antibiotic (b) Analgesic (c) Antacid (d) Antiseptic
अपच का उपचार करने के लिए निम्न में से किस औषधि का उपयोग होता है?
(a) एंटीबायोटिक (प्रतिजैविक)
(b) ऐनालजेसिक (पीड़ाहारी)
(c) ऐन्टैसिड
(d) एंटीसेप्टिक (प्रतिरोधी)
Answer
(c) Antacid
(c) ऐन्टैसिड
Question 5:
Write word equations and then balanced equations for the reaction taking place when –
(a) dilute sulphuric acid reacts with zinc granules.
(b) dilute hydrochloric acid reacts with magnesium ribbon.
(c) dilute sulphuric acid reacts with aluminium powder.
(d) dilute hydrochloric acid reacts with iron filings.
निम्न अभिक्रिया के लिए पहले शब्द-समीकरण लिखिए तथा उसके बाद संतुलित समीकरण लिखिए:
(a) तनु सल्फ्यूरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है|
(b) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है|
(c) तनु सल्फ्यूरिक अम्ल एलुमिनियम चूर्ण के साथ अभिक्रिया करता है|
(d) तनु हाइड्रोक्लोरिक अम्ल लौह के रेतन के साथ अभिक्रिया करता है|
Answer
(a) H2SO4 (aq) + Zn (s) → ZnSO4 (aq) + H2 (g)
(b) 2HCl (aq) + Mg (s) → MgCl2 (aq) + H2 (g)
(c) 3H2SO4 (aq) + 2Al (s) → Al2(SO4)3 (aq) + 3H2 (g)
(d) 6HCl (aq) + 2Fe (s) → 2FeCl3 (aq) + 3H2 (g)
Question 6:
Compounds such as alcohols and glucose also contain hydrogen but are not categorised as acids. Describe an Activity to prove it.
एल्कोहॉल एवं ग्लूकोज जैसे यौगिकों में भी हाइड्रोजन होते हैं लेकिन इनका वर्गीकरण अम्ल की तरह नहीं होता है| एक क्रियाकलाप द्वारा इसे साबित कीजिये|
Answer
Take solutions of glucose, alcohol, hydrochloric acid, and sulphuric acid in separate beakers. Fix two nails on a cork and place it in each beaker. Connect the nails to a battery and a bulb. The bulb glows with acids but not with glucose or alcohol. This shows that acids produce ions in water that conduct electricity, while glucose and alcohol do not. Hence, though they contain hydrogen, they are not acids.
ग्लूकोज, एल्कोहॉल, हाइड्रोक्लोरिक अम्ल तथा सल्फ्यूरिक अम्ल के जलीय विलयन लें। प्रत्येक में दो कीलों को कॉर्क पर लगाकर डुबोएँ और उन्हें बैटरी तथा बल्ब से जोड़ें। अम्लों वाले विलयनों में बल्ब जलेगा, लेकिन ग्लूकोज एवं एल्कोहॉल वाले में नहीं। यह दर्शाता है कि अम्ल जल में आयन उत्पन्न करते हैं, जिससे विद्युत प्रवाह होता है। जबकि ग्लूकोज एवं एल्कोहॉल में हाइड्रोजन होते हुए भी वे आयन नहीं बनाते।
Question 7:
Why does distilled water not conduct electricity, whereas rain water does?
आसवित जल विद्युत् का चालक क्यों नहीं होता जबकि वर्षा जल होता है?
Answer
Distilled water cannot conduct electricity because it does not contain ions while rain water conducts electricity as it contains ions due presence of dissolved salts in it.
आसवित जल विद्युत् का चालक नहीं होता है क्योंकि इसमें आयन उपस्थित नहीं होते हैं जबकि वर्षा जल विद्युत् का चालन करता है क्योंकि इसके आयनों में विघटित लवण की मौजूद होते हैं|
Question 8:
Why do acids not show acidic behaviour in the absence of water?
जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय क्यों नहीं होता है?
Answer
Acids do not show acidic behaviour in the absence of water because the dissociation of hydrogen ions from an acid occurs in the presence of water only.
जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय नहीं होता है क्योंकि अम्ल से हाइड्रोजन का विघटन केवल जल की उपस्थिति में उत्पन्न होता है|
Question 9:
Five solutions A,B,C,D and E when tested with universal indicator showed pH as 4,1,11,7 and 9, respectively. Which solution is
(a) neutral?
(b) strongly alkaline?
(c) strongly acidic?
(d) weakly acidic?
(e) weakly alkaline?
Arrange the pH in increasing order of hydrogen-ion concentration.
पाँच विलयनों A, B, C, D, व E की जब सार्वत्रिक सूचक से जाँच की जाती है तो pH के मान क्रमशः 4, 1, 11, 7 एवं 9 प्राप्त होते हैं| कौन सा विलयन:
(a) उदासीन है?
(b) प्रबल क्षारीय है?
(c) प्रबल अम्लीय है?
(d) दुर्बल अम्लीय है?
(e) दुर्बल क्षारीय है?
pH के मानों को हाइड्रोजन आयन की सांद्रता के आरोही क्रम में व्यवस्थित कीजिये|
Answer
(a) Neutral →Solution D with pH 7
(b) Strongly alkaline →Solution C with pH 11
(c) Strongly acidic →Solution B with pH 1
(d) Weakly acidic →Solution A with pH 4
(e) Weakly alkaline →Solution E with pH 9
The pH can be arranged in the increasing order of the concentration of hydrogen ions as: 11 < 9 < 7 < 4 < 1.
(a) उदासीन → विलयन D के साथ pH 7
(b) प्रबल क्षारीय → विलयन C के साथ pH 11
(c) प्रबल अम्लीय → विलयन B के साथ pH 1
(d) दुर्बल अम्लीय → विलयन A के साथ pH 4
(e) दुर्बल क्षारीय → विलयन E के साथ pH 9
pH के मानों को हाइड्रोजन आयन की सांद्रता के आरोही क्रम में व्यवस्थित करने पर: 11 < 9 < 7 < 4 < 1.
Question 10:
Equal lengths of magnesium ribbons are taken in test tubes A and B. Hydrochloric acid (HCl) is added to test tube A, while acetic acid (CH3COOH) is added to test tube B. Amount and concentration taken for both the acids are same. In which test tube will the fizzing occur more vigorously and why?
परखनली ‘A’ एवं ‘B’ में समान लंबाई की मैग्नीशियम की पट्टी लीजिए| परखनली ‘A’ में हाइड्रोक्लोरिक अम्ल (HCl) तथा परखनली ‘B’ में एसिटिक अम्ल (CH_3COOH) डालिए| किस परखनली में अधिक तेजी से बुदबुदाहट होगी तथा क्यों?
Answer
The fizzing will occur strongly in test tube A, in which hydrochloric acid (HCl) is added. This is because HCl is a stronger acid than CH3COOH and therefore produces hydrogen gas at a faster speed due to which fizzing occurs.
परखनली ‘A’ में अधिक तेजी से बुदबुदाहट होगी जिसमे हाइड्रोक्लोरिक अम्ल (HCl) है| ऐसा इसलिए होता है क्योंकि HCl अम्ल CH3COOH अम्ल की तुलना में अधिक प्रबल है| इस प्रकार तीव्र गति में हाइड्रोजन गैस उत्पन्न होता है जिस कारण बुदबुदाहट उत्पन्न होता है|
vNCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Question 11:
Fresh milk has a pH of 6. How do you think the pH will change as it turns into curd? Explain your answer.
ताजे दूध के pH का मान 6 होता है| दही बन जाने पर इसके pH के मान में क्या परिवर्तन होगा? अपना उत्तर समझाइए|
Answer
The pH of milk is 6. As it changes to curd, the pH will reduce because curd is acidic in nature. The acids present in it decrease the pH.
दूध का pH का मान 6 होता है| जैसे यह दही में परिवर्तित होता है, pH का मान घट जाता है| इसमें मौजूद अम्ल pH के मान को कम करता है|
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Question 12:
A milkman adds a very small amount of baking soda to fresh milk.
(a) Why does he shift the pH of the fresh milk from 6 to slightly alkaline?
(b) Why does this milk take a long time to set as curd?
एक ग्वाला ताजे दूध में थोड़ा बेकिंग सोडा मिलाता है|
(a) ताजा दूध के pH के मान को 6 से बदलकर थोड़ा क्षारीय क्यों बना देता है?
(b) इस दूध को दही बनने में अधिक समय क्यों लगता है?
Answer
(a) The milkman shifts the pH of the fresh milk from 6 to slightly alkaline because in alkaline condition, milk does not set as curd easily.
(b) Since this milk is slightly basic than usual milk, acids produced to set the curd are neutralized by the base. Therefore, it takes a longer time for the curd to set.
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Question 13:
Plaster of Paris should be stored in a moisture-proof container. Explain why?
प्लास्टर ऑफ़ पेरिस को आर्द्र-रोधी बर्तन में क्यों रखा जाना चाहिए| इसकी व्याख्या कीजिये|
Answer
The Plaster of Paris should be stored in a moisture-proof container as it absorbs water from moisture and turn into hard substance (Gypsum) as shown in following chemical equation.
प्लास्टर ऑफ़ पेरिस को आर्द्र-रोधी बर्तन में रखा जाना चाहिए क्योंकि यह नमी से जल अवशोषित करता है तथा जिप्सम बनकर कठोर ठोस पदार्थ में बदल जाता है| इसे निम्नलिखित समीकरण द्वारा दर्शाया गया है:

NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Question 14:
What is a neutralisation reaction? Give two examples.
उदासीनीकरण अभिक्रिया क्या है? दो उदाहरण दीजिये|
Answer
A reaction in which an acid and base react with each other to give a salt and water is termed as neutralization reaction.For Example:
अम्ल एवं क्षारक की अभिक्रिया के परिणामस्वरुप लवण तथा जल प्राप्त होते हैं जिसे उदासीनीकरण अभिक्रिया कहते हैं|
(i) NaOH + HCl → NaCl + H2O
(ii) HNO3 + KOH → KNO3 + H2O
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण
Question 15:
Give two important uses of washing soda and baking soda.
धोने का सोडा एवं बेकिंग सोडा के दो-दो प्रमुख उपयोग बताइए|
Answer
Two important uses of washing soda are:
(1) It is used in glass, soap, and paper industries.
(2 It is used to remove permanent hardness of water.
Two important uses of baking soda are:
(1) It is used as baking powder. Baking powder is a mixture of baking soda and a mild acid known as tartaric acid. When it is heated or mixed in water, it releases CO2 that makes bread or cake fluffy.
(2) It is used in soda-acid fire extinguishers.
धोने का सोडा के दो प्रमुख उपयोग निम्नलिखित हैं:
(i) इसका उपयोग काँच, साबुन एवं कागज उद्योगों में होता है|
(ii) जल की स्थायी कठोरता को हटाने के लिए इसका उपयोग होता है|
बेकिंग सोडा के दो उपयोग निम्नलिखित हैं:
(i) बेकिंग पाउडर बनाने में, जो बेकिंग सोडा (सोडियम हाइड्रोजनकार्बोनेट) एवं टार्टरिक अम्ल जैसा एक मंद खाद्य अम्ल का मिश्रण है| जब बेकिंग पाउडर को गर्म किया जाता है या जल में मिलाया जाता है तो इस अभिक्रिया से उत्पन्न कार्बन डाइऑक्साइड के कारण यह पावरोटी या केक को स्पंजी बना देता है|
(ii) इसका उपयोग सोडा-अम्ल अग्निशामक में भी किया जाता है|
NCERT Solution of Class 10 Science Ch-2 Acids Bases and Salts अम्ल, क्षारक एवं लवण

