Important Questions for Class 10 Science Chapter 2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण

NCERT Solutions for Class 10 Science Chapter 2
Thank you for reading this post, don't forget to subscribe!1 Marks
Question 1:
The following table shows the pH values of four solutions A, B, C and D on a pH scale :
निम्नलिखित तालिका में pH स्केल पर चार विलयनों A, B, C और D के pH मान दर्शाए गए है:
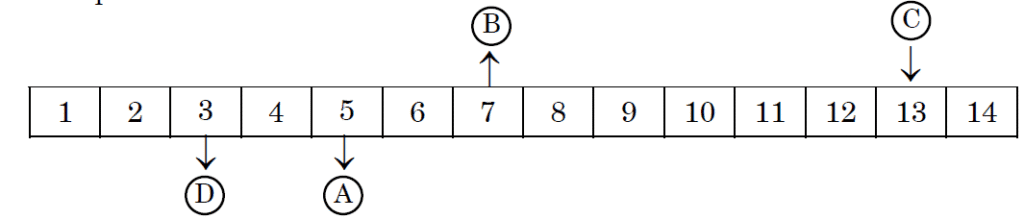
The solutions A, B, C and D respectively are of a
(A) Strong acid, weak acid, neutral, strong base
(B) Weak acid, neutral, weak base, strong base
(C) Weak acid, neutral, strong base, weak base
(D) Weak acid, neutral, strong base, strong acid
ये चारों विलयन A, B, C और D क्रमशः है:
(a) प्रबल अम्ल, दुर्बल अम्ल, उदासीन, प्रबल क्षारक
(b) दुर्बल अम्ल, उदासीन, दुर्बल क्षारक, प्रबल क्षारक
(c) दुर्बल अम्ल, उदासीन, प्रबल क्षारक,दुर्बल क्षारक
(d) दुर्बल अम्ल, उदासीन, प्रबल क्षारक, प्रबल अम्ल
Question 2:
Consider the following reactions :
(i) Dilute hydrochloric acid reacts with sodium hydroxide.
(ii) Magnesium oxide reacts with dilute hydrochloric acid.
(iii) Carbon dioxide reacts with sodium hydroxide.
It is found that in each case :
(A) Salt and water is formed.
(B) Neutral salts are formed.
(C) Hydrogen gas is formed.
(D) Acidic salts are formed.
निम्नलिखित अभिक्रियाओं पर विचार कीजिए:
(i) तनु हाइड्रोक्लोरिक अम्ल, सोस्डयम हाइड्रॉक्ट्साइड से अभिक्रिया करता है ।
(ii) मैग्नीशियम ऑक्साइड, तनु हाइड्रोक्लोरिक अम्ल से अभिक्रिया करता है ।
(iii) कार्बन डाइॉक्साइड, सोस्डयम हाइड्रॉक्ट्साइड से अभिक्रिया करती है ।
यह पाया जाता है कि प्रत्येक प्रकरण में :
(A) लवण और जल बनता है ।
(B) उदासीन लवण बनते हैं ।
(C) हाइड्रोजन गैस बनती है ।
(D) अम्लीय लवण बनते हैं ।
Question 3:
You have three aqueous solutions A, B and C as given below :
A – Potassium nitrate
B – Ammonium chloride
C – Sodium carbonate
The ascending order of the pH of these solutions is :
(A) A < B < C
(B) B < C < A
(C) C < A < B
(D) B < A < C
आपके पास नीचे दिए अनुसार तीन लवणों A, B और C के जलीय विलयन हैं :
A – पोटैशियम नाइट्रेट
B – अमोनियम क्लोराइड
C – सोडियम कार्बोनेट
इन विलयनों के pH का आरोही (बढ़ता) क्रम है :
(A) A < B < C
(B) B < C < A
(C) C < A < B
(D) B < A < C
Question 4:
Juice of tamarind turns blue litmus to red. It is because of the presence of a chemical compound called
(A) Acetic acid
(B) Methanoic acid
(C) Oxalic acid
(D) Tartaric acid
इमली का रस नीले लिटमस को लाल कर देता है। इसका कारण एक रासायनिक यौगिक की उपस्थिति है:
(A) एसीटिक अम्ल
(B) मेथेनॉइक अम्ल
(C) ऑक्सैलिक अम्ल
(D) टार्टरिक अम्ल
Question 5:
The water of crystallization is present in
निम्नलिखित में से किनमें क्रिस्टलन का जल उपस्थित है?
(i) Bleaching Powder विरंजक चूर्ण
(ii) Plaster of Paris प्लास्टर ऑफ पेरिस
(iii) Washing Soda धोने का सोडा
(iv) Baking Soda बेकिंग सोडा
(A) (ii) and (iv)
(B) (ii) and (iii)
(C) (i) and (iii)
(D) (i) and (iv)
Important Questions for Class 10 Science Ch-2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण
2 Marks
Question 1:
A substance ‘X’ is a white powder and on mixing with water changes to a hard solid mass ‘Y’ containing 2 molecules of water of crystallisation. Identify ‘X’ & ‘Y’ and write the chemical equation when ‘X’ is mixed with water to form Y.
पदार्थ ‘X’ एक सफेद पाउडर है और यह जल के साथ मिलाने पर कठोर ठोस ‘Y’ में परिवर्तित होता है जिससे 2 अणु क्रिस्टलन का जल है। ‘X’ और ‘Y’ को पहचाने और जब ‘X’ पानी के साथ मिलकर ‘Y’ बनता है, रसायनिक समीकरण लिखें।
Question 2:
Write the chemical name and molecular formula of Plaster of Paris. Why should it be stored in a moisture proof container? प्लास्टर ऑफ पेरिस का रासायनिक नाम और आण्विक सूत्र लिखिए। इसका भंडारण नमी रोधी पत्रों में क्यों किया जाना चाहिए।
Answer
Chemical name: Calcium sulphate hemihydrate
Molecular formula: CaSO₄·½H₂O
Plaster of Paris reacts with moisture (water) present in the air and converts into gypsum (CaSO₄·2H₂O). Due to this reaction, it becomes hard and loses its setting property. Therefore, it should be stored in a moisture-proof container.
रासायनिक नाम: कैल्शियम सल्फेट अर्धजलयोजित
आण्विक सूत्र: CaSO₄·½H₂O
इसे नमीरोधी पात्र में इसलिए रखा जाता है क्योंकि यह वायु की नमी से अभिक्रिया करके जिप्सम (CaSO₄·2H₂O) में बदल जाता है और अपनी जमने की क्षमता खो देता है।
Question 3:
What is a neutralisation reaction ? Write the chemical equation for a neutralisation reaction and write the name of the salt produced.
उदासीनीकरण किसे कहते है? किसी उदासीनीकरण अभिक्रिया का रासायनिक समीकरण लिखिए और बनने वाले लवण के नाम का उल्लेख कीजिए।
Answer
A neutralisation reaction is a reaction in which an acid reacts with a base to form salt and water.
HCl + NaOH → NaCl + H₂O
Name of the salt formed: Sodium chloride
जब कोई अम्ल किसी क्षार से अभिक्रिया करके लवण और जल बनाता है, तो उसे उदासीनीकरण अभिक्रिया कहते हैं।
HCl + NaOH → NaCl + H₂O
बनने वाला लवण: सोडियम क्लोराइड
Important Questions for Class 10 Science Ch-2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण
3 Marks
Question 1:
(a) Write the name and chemical formula of a sodium compound which is sometimes added for faster cooking. How is it produced from sodium chloride as one of the raw materials ? Give chemical equation for the reaction involved.
(b) The compound mentioned in (a) above is also an ingredient of antacids. Why ?
(क) सोडियम के उस यौगिक का नाम और रासायनिक सूत्र लिखिए जिसका उपयोग कभी-कभी भोजन शीघ्र पकाने के लिए किया जाता है । सोडियम क्लोराइड को एक कच्ची सामग्री के रुप में लेकर इस यौगिक का निर्माण किस प्रकार किया जाता है ? होने वाली अभिक्रिया का रासायनिक समीकरण दीजिए ।
(ख) ऊपर (क) में उल्लिखित यौगिक ऐन्टैसिड का एक संघटक भी है। क्यों ?
Answer
(a) Name of sodium compound: Sodium hydrogen carbonate (Baking soda)
Chemical formula: NaHCO₃
Use in cooking:
It is sometimes added for faster cooking because it makes the food medium alkaline and helps soften food (like pulses).
Production from sodium chloride:
Sodium hydrogen carbonate is produced from sodium chloride by the Solvay process.
Chemical equation:
NaCl + NH3 + H2O + CO2 → NaHCO3↓ + NH4Cl
सोडियम के उस यौगिक का नाम और रासायनिक सूत्र
जिसका उपयोग कभी-कभी भोजन को शीघ्र पकाने के लिए किया जाता है:
नाम: सोडियम हाइड्रोजन कार्बोनेट (बेकिंग सोडा)
रासायनिक सूत्र: NaHCO₃
सोडियम क्लोराइड को एक कच्ची सामग्री के रूप में लेकर निर्माण:
सोडियम हाइड्रोजन कार्बोनेट का निर्माण सॉल्वे विधि द्वारा किया जाता है।
रासायनिक समीकरण:
NaCl + NH3 + H2O + CO2 → NaHCO3↓ + NH4Cl
(b) Sodium hydrogen carbonate is basic in nature, so it neutralizes excess acid in the stomach and gives relief from acidity and indigestion.
सोडियम हाइड्रोजन कार्बोनेट क्षारीय प्रकृति का होता है, इसलिए यह पेट में उपस्थित अधिक अम्ल (HCl) को निष्क्रिय कर देता है और अम्लता से राहत देता है।
Question 2:
Consider the following salts : (i) XCl (ii) NH4Y (iii) ZCO3 Answer the following questions giving reason in each case.
(a) If ‘X’ is sodium, what is the pH of XCl ?
(b) If ‘Y’ is sulphate, what colour would the aqueous solution of NH4Y give when a few drops of universal indicator are added to it ?
(c) If ‘Z’ is calcium, what would be the change in colour in blue litmus paper when a drop of ZCO3 is poured on it ?
नीचे दिए गए लवणों पर विचार कीजिए:
(i) XCl (ii) NH4Y (iii) ZCO3
प्रत्येक प्रकरण में कारण देते हुए नीचे दिए गए प्रश्नों के उत्तर दीजिए।
(क) यदि ‘X’ सोडियम है तो क्या है?
(ख) यदि ‘Y’ सल्फेट है, तो NH4Y के जलीय विलयन में सार्वत्रिक सूचक की कुछ बूँदे डालने पर विलयन का रंग क्या होगा ?
(c) यदि ‘Z’ कैल्शियम है, तो नीले लिटमस पत्र पर ZCO3 की एक बूँद डालने पर उसके रंग में क्या परिवर्तन होगा ?
Answer
(a) If X = Sodium, then XCl = NaCl (Sodium chloride).
NaCl is formed from a strong acid (HCl) and a strong base (NaOH). Therefore, it is a neutral salt.
pH = 7
Reason: Salt formed from a strong acid and strong base is neutral in nature.
यदि X = सोडियम, तो XCl = NaCl होगा।
यह एक प्रबल अम्ल (HCl) और प्रबल क्षार (NaOH) से बना है, इसलिए इसका pH = 7 (उदासीन) होगा।
(b) If Y = Sulphate (SO₄²⁻), then NH₄Y = (NH₄)₂SO₄ (Ammonium sulphate).
Ammonium sulphate is formed from a strong acid (H₂SO₄) and a weak base (NH₄OH). Hence, it is acidic in nature.
Colour with universal indicator: Greenish-yellow (pH less than 7)
Reason: Salt of strong acid and weak base is acidic.
यदि Y = सल्फेट, तो NH₄Y = (NH₄)₂SO₄ अमोनियम सल्फेट होगा।
यह अम्लीय लवण है, इसलिए सार्वत्रिक सूचक डालने पर इसका रंग पीला-हरा (अम्लीय) होगा।
(c) If Z = Calcium, then ZCO₃ = CaCO₃ (Calcium carbonate).
Calcium carbonate is a salt of strong base (Ca(OH)₂) and weak acid (H₂CO₃). Therefore, it is basic in nature.
Effect on blue litmus paper: No change (it remains blue).
Reason: Basic substances do not change the colour of blue litmus paper.
यदि Z = कैल्शियम, तो ZCO₃ = CaCO₃ (कैल्शियम कार्बोनेट) होगा।
यह क्षारीय प्रकृति का है, इसलिए नीला लिटमस पत्र नीला ही रहेगा (कोई परिवर्तन नहीं)।
Important Questions for Class 10 Science Ch-2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण
Question 3:
(i) The pH of a sample of tomato juice is 4.6. How is this juice likely to be in taste? Give reason to justify your answer.
(ii) How do we differentiate between a strong acid and a weak base in terms of ion-formation in aqueous solutions?
(iii) The acid rain can make the survival of aquatic animals difficult. How?
(i) टमाटर के जूस के किसी नमूने का pH 4.6 hai। इस जूस का स्वाद कैसा होना चाहिए? अपने उत्तर का कारण दीजिए।
(ii) हम किसी प्रबल अम्ल और दुर्बल क्षारक के बीच विभेदन जलीय विलयनओं में आयन बनने के पदों में किस प्रकार करते हैं?
(iii) अम्लीय वर्षा का जल जलीय जंतुओं की उत्तर-जीविता को कठिन बना देती है। ऐसा किस प्रकार होता है?
Important Questions for Class 10 Science Ch-2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण
Case-based Questions (4 Marks)
Question 1:
Seawater contains many salts dissolved in it. Common salt is separated from these salts. Deposits of solid salt are also found in several parts of the world. These large crystals are often brown due to impurities. This is called rock salt and is mined like coal. The common salt is an important raw material for chemicals of daily use.
(a) Write balanced chemical equations to show the products formed during electrolysis of brine.
(b) List two uses of any one product obtained during electrolysis of brine.
(c) (i) A mild non-corrosive basic salt ‘A’, used for faster cooking, is strongly heated to produce a compound ‘B’, that is used for removing permanent hardness of water. Identify A and B and also write the equation for the reaction that occurs when A is heated.
OR
(c) (ii) Define water of crystallisation. Give two examples of salts that have water of crystallisation.
समुद्री जल में कई प्रकार के लवण घुले होते हैं । साधारण नमक को इन लवणों से पृथक किया जाता है । विश्व के कई भागों में भी ठोस लवण का निक्षेप होता है । बड़े आकार के यह क्रिस्टल प्राय: अपद्रव्यों (अशुद्धियों) के कारण भूरे रंग के होते हैं । इसे खनिज नमक कहते हैं । इसका खनन भी कोयले की भांति होता है । साधारण नमक दैनिक जीवन में उपयोग होने वाले रसायनों के के लिए एक महत्त्वपूर्ण कच्ची सामग्री है ।
(क) लवण-जल (ब्राइन) के विद्युत-अपघटन से उत्पन्न उत्पादों को दर्शाने लिए संतुलित रासायनिक समीकरण लिखिए।
(ख) लवण-जल (ब्राइन) के विद्युत -अपघटन से प्राप्त किसी भी एक उत्पाद के दो उपयोगों की सूची बनाइए ।
(ग) (i) किसी दुर्बल असंक्षारक क्षारीय लवण ‘A’ का उपयोग खाने को शीघ्रता से पकाने में किया जाता है । इसे गर्म करने पर कोई यौगिक ‘B’ बनता है जिसका उपयोग जल की स्थायी कठोरता को दूर करने में किया जाता है । A और B को पहचानिए तथा A को गर्म करने पर होने वाली अभिक्रिया का समीकरण भी लिखिए।
अथवा
(ग) (ii) क्रिस्टल के जल की परिभाषा लिखिए। उन दो लवणों का उदाहरण दीजिए जिनमें क्रिस्टल का जल होता है ।
5 Marks
Question 1:
Name and state in brief the process used to obtain sodium hydroxide from brine. In this process, along with the main product (i.e., sodium hydroxide), two gases A and B are also produced at the two electrodes. Name A and B specifying the name of their respective electrodes. One of these gases, when reacting with dry calcium hydroxide, produces a compound C which is used as an oxidising agent in many chemical industries as well as to make drinking water free from germs. Name C and write the chemical equation for the reaction in its formation.
लवण जल से सोडियम हाइड्रॉक्साइड प्राप्त करने की प्रक्रिया का नाम लिखिए और संक्षेप में इसका उल्लेख कीजिए। इस प्रक्रिया में मुख्य उत्पाद (सोडियम हाइड्रॉक्साइड) के साथ ही इलेक्ट्रोडों पर दो गैस A और B भी उत्पन्न होती हैं। A और B के नामों का उल्लेख उनके इलेक्ट्रोडों के नामों सहित कीजिए। इनमें से एक गैस शुष्क कैल्सियम हाइड्रॉक्साइड से अभिक्रिया करके कोई यौगिक C निर्मित करती है जिसका उपयोग कई रासायनिक उद्योगों में ऑक्सीकारक के रूप में तथा पेय जल को रोगाणु मुक्त बनाने में किया जाता है। यौगिक C का नाम लिखिए तथा इसके निर्मित होने में होने वाली अभिक्रिया का रासायनिक समीकरण लिखिए।
Answer
Name of the process: Chlor-alkali process
Brief description of the process:
When an aqueous solution of sodium chloride (brine) is electrolysed, sodium hydroxide is formed in the solution. During electrolysis, gases are released at both electrodes.
Products formed:
At cathode: Hydrogen gas (A)
At anode: Chlorine gas (B)
In solution: Sodium hydroxide (NaOH)
Electrode reactions:
Cathode:
2H2O+2e– → H2 + 2OH
Anode:
2Cl → Cl2 + 2e−
Gas reacting with dry calcium hydroxide:
Chlorine gas (B) reacts with dry calcium hydroxide to form compound C.
Name of compound C: Bleaching powder (Calcium oxychloride)
Use of compound C:
(i) Used as an oxidising agent in chemical industries
(ii) Used to disinfect drinking water
Chemical equation for formation of C:
Ca(OH)2 + Cl2 → CaOCl2 + H2O
प्रक्रिया का नाम: क्लोर-क्षार (Chlor-alkali) प्रक्रिया
संक्षिप्त विवरण:
जब सोडियम क्लोराइड के जलीय विलयन (लवण जल) का विद्युत-अपघटन किया जाता है, तो विलयन में सोडियम हाइड्रॉक्साइड (NaOH) बनता है तथा दोनों इलेक्ट्रोडों पर गैसें निकलती हैं।
इलेक्ट्रोडों पर उत्पन्न गैसें:
गैस A: हाइड्रोजन (H₂) — कैथोड पर
गैस B: क्लोरीन (Cl₂) — ऐनोड पर
यौगिक C का निर्माण:
क्लोरीन गैस (B) जब शुष्क कैल्शियम हाइड्रॉक्साइड से अभिक्रिया करती है, तो यौगिक C बनता है।
यौगिक C का नाम: ब्लीचिंग पाउडर (Calcium oxychloride)
उपयोग:
(i) रासायनिक उद्योगों में ऑक्सीकारक के रूप में
(ii) पीने के जल को रोगाणु-मुक्त करने के लिए
यौगिक C के निर्माण की रासायनिक समीकरण:
Ca(OH)2 + Cl2 → CaOCl2 + H2O
Question 2:
When dry crystals of ferrous sulphate were heated in a dry boiling tube, some tiny water droplets were observed in the tube after some time.
(i) State the source of these water droplets.
(ii) Write the color change observed during heating.
(iii) Write the balanced chemical equation of the reaction that occurs during heating.
(iv) How many water molecules are attached per formula unit of ferrous sulphate crystal?
(v) Write the molecular formula of crystalline form (I) copper sulphate and (II) sodium carbonate.
जब फेरस सल्फेट के शुष्क क्रिस्टलों को शुष्क क्वथन नली में गर्म किया गया, तो कुछ समय पश्चात नली में जल की सूक्ष्म बूँदें दिखाई दीं।
(i) इन सूक्ष्म बूँदों के स्रोत का उल्लेख कीजिए।
(ii) गर्म करते समय प्रेक्षण किए जाने वाले रंग में परिवर्तन को लिखिए।
(iii) गर्म करते समय होने वाली अभिक्रिया का संतुलित रासायनिक समीकरण लिखिए।
(iv) फेरस सल्फेट क्रिस्टल के एक सूत्र इकाई में जल के कितने अणु उपस्थित होते हैं?
(v) (I) कॉपर सल्फेट और (II) सोडियम कार्बोनेट के क्रिस्टलीय रूप के आण्विक सूत्र लिखिए।
Answer
(i) The water droplets come from the water of crystallisation present in ferrous sulphate crystals.
ये सूक्ष्म जल बूँदें फेरस सल्फेट के क्रिस्टलों में उपस्थित जलयोजक जल से प्राप्त होती हैं।
(ii) Colour change observed during heating
\(\quad\) a. Green ferrous sulphate crystals
\(\quad\) b. turn white (on losing water)
\(\quad\) c. and finally become brown (due to formation of ferric oxide)
(ii) गर्म करते समय देखे गए रंग में परिवर्तन
a. फेरस सल्फेट का रंग हरा होता है।
b. गर्म करने पर यह सफेद हो जाता है।
c. अधिक गर्म करने पर यह भूरा (फेरिक ऑक्साइड बनने के कारण) हो जाता है।
(iii) Balanced chemical equation of the reaction
First, loss of water:On further heating:
जलयोजक जल का निकलना:
अधिक गर्म करने पर:
(iv) Number of water molecules attached per formula unit = 7 water molecules
फेरस सल्फेट के एक सूत्रक इकाई में कितने जल अणु जुड़े होते हैं? = 7 जल अणु
(v) Molecular formula of crystalline forms
(I) Copper sulphate: (II) Sodium carbonate:
(v) क्रिस्टलीय रूप का आणविक सूत्र
(I) कॉपर सल्फेट:
(II) सोडियम कार्बोनेट:
Important Questions for Class 10 Science Ch-2 Acids, Bases and Salts अम्ल, क्षारक एवं लवण

